Приблизително за един на всеки сто души храната, съдържаща дори и най-малкото количество глутен, може да причини огромна болка.
Въпреки че ефектът на доминото на имунологичните реакции може да бъде проследен до техните генетични корени , редица допринасящи фактори също са включени, което затруднява картографирането на точната верига от събития, които причиняват появата на непоносимост към глутен.
Използвайки трансгенни мишки, международен екип, ръководен от учени от университета Макмастър в Канада, идентифицира решаващата роля, която играят самите клетки, изграждащи лигавицата на червата, описвайки основна стъпка, която може да доведе до нови терапии.
Цьолиакията по същество е автоимунно разстройство, предизвикано от наличието на група структурни протеини, известни като глутен в червата.
Яденето на почти всичко, направено с пшеница, ечемик или ръж – което означава повечето печени продукти, хляб и тестени изделия – излага хората със заболяването на риск от подуване на корема, болка, диария, запек и понякога рефлукс и повръщане.
В момента единственият начин да се избегнат симптомите е да се избягват храните, които ги предизвикват.
„Единственият начин, по който можем да лекуваме цьолиакия днес, е като напълно премахнем глутена от диетата“, казва гастроентерологът на McMasters Елена Верду. „Това е трудно осъществимо и експертите са съгласни, че диетата без глутен е недостатъчна.“
Около 90 процента от хората, диагностицирани със заболяването, носят чифт гени, които кодират протеин, наречен HLA-DQ2.5 . От останалите 10 процента повечето имат подобен протеин, наречен HLA-DQ8.
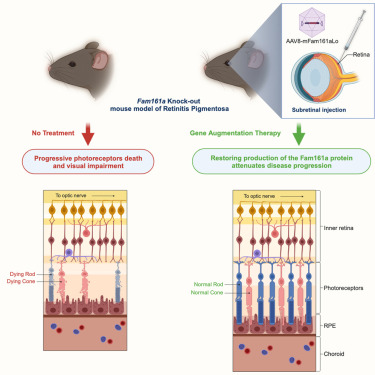
Подобно на други видове „HLA“ (или човешки левкоцитен антиген ) протеини, протеините държат парчета от паднали нашественици високо като зловещи трофеи върху клас имунни клетки , предупреждавайки другите защитни тъкани да бъдат нащрек.
В конкретния случай на HLA-DQ2.5 и HLA-DQ8, протеините са оформени да държат парчета глутенов пептид, които са устойчиви на смилане, инструктирайки убийствените Т-клетки да тръгнат на лов.
За съжаление, тези инструкции не са най-ясни за разграничаване между заплаха и подобни на вид материали в нашето тяло, което означава, че тези с гените са изложени на риск от различни автоимунни състояния.
Не всеки , който експресира HLA-DQ2.5 или HLA-DQ8, обаче ще развие имунно разстройство като целиакия. За да се случи това, тези накъсани парчета глутен първо трябва да бъдат пренесени през чревната стена от транспортиращ ензим , който се свързва с пептида и го променя по начини, за да го направи още по-разпознаваем.
Клетките в чревната стена са отговорни за освобождаването на този транспортиращ ензим в червата, така че очевидно имат критична роля в ранните стадии на заболяването. Известно е също така, че експресират семейството протеини, към които принадлежат HLA-DQ2.5 и HLA-DQ8, които обикновено се регулират от възпалителни реакции в червата.
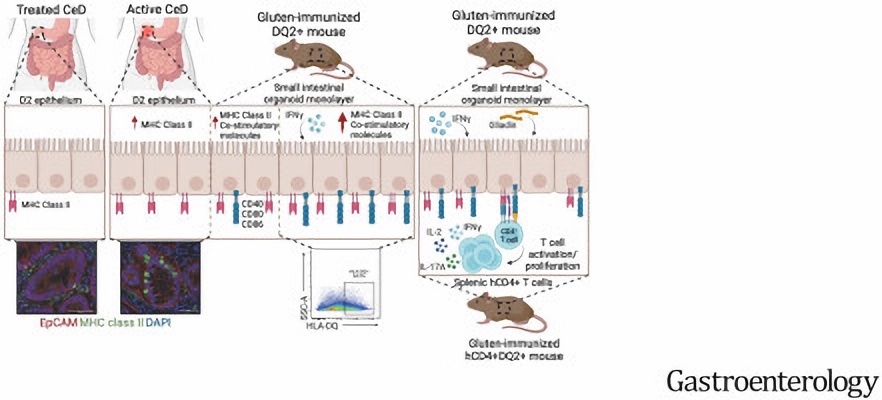
Това, което не е ясно, е как тази сцена за хора с целиакия всъщност функционира в рамките на самата патология.
За да се съсредоточи върху тази важна връзка във веригата, изследователският екип провери два пъти експресията на основния имунен комплекс в клетките, покриващи червата на хора с лекувана и нелекувана цьолиакия, и при мишки с човешки гени за HLA-DQ2. 5.
След това те създадоха функционални живи модели на червата, наречени органоиди , използвайки чревните клетки на мишката, за да проучат отблизо експресията на техните имунни протеини, подлагайки ги на възпалителни тригери, както и на предварително усвоен и непокътнат глутен.
„Това ни позволи да стесним конкретната причина и следствие и да докажем точно дали и как протича реакцията“, казва биомедицинският инженер от McMasters Тохид Дидар.
От това стана ясно, че клетките, покриващи червата, не са просто пасивни наблюдатели, страдащи от съпътстващи щети в погрешни усилия да се отърве тялото от глутена – те са ключови агенти, представляващи смес от глутенови фрагменти, разградени от чревни бактерии и транспортиращи ензими към специфични за глутен имунни клетки от първа ръка.
Познаването на типовете участващи тъкани и тяхното усилване чрез наличието на възпалителни микроби дава на изследователите нов списък от цели за бъдещи лечения, което потенциално позволява на милиони хора по света да се насладят на сладкиши с глутен или два без риск от дискомфорт.
Това изследване е публикувано в Gastroenterology .
Референции
-
Цьолиакия.
Ланцет. 2022 г.; 399 : 2413-2426
-
Цьолиакия.
Nat Rev Dis Primers. 2019 г.; 5 : 3
-
Идентифициране на тъканна трансглутаминаза като автоантиген на целиакия.
Nat Med. 1997 г.; 3 : 797-801
-
Поява на адаптивна имунна парадигма за обяснение на цьолиакия: гледна точка към нови доказателства и последици за бъдещи интервенции и диагностика.
Expert Rev Clin Immunol. 2022 г.; 18 : 75-91
-
Кофактори, микроби и имуногенетика при целиакия за насочване на нови подходи за диагностика и лечение.
Гастроентерология. 2021 г.; 161 : P1395-P1411.E4
-
Доказателство за първична връзка на целиакия с конкретен HLA-DQ α/β хетеродимер.
J Exp Med. 1989 г.; 169 : 345-350
-
Т клетки от лигавицата на тънките черва на DR4, DQ7/DR4. DQ8 пациент с цьолиакия преференциално разпознава глиадин, когато се представя от DQ8.
Hum Immunol. 1994 г.; 41 : 285-291
-
Изчерпателно, количествено картографиране на Т клетъчни епитопи в глутен при целиакия.
Sci Transl Med. 2010 г.; 2 : 41ra51
-
Идентифициране и анализ на многовалентни протеолитично устойчиви пептиди от глутен: последици за целиакия.
J Proteome Res. 2005 г.; 4 : 1732-1741
-
Структурна основа за непоносимост към глутен при целиакия.
Наука (1979). 2002 г.; 297 : 2275-2279
-
Механизми, чрез които чревните микроорганизми влияят върху хранителната чувствителност.
Nat Rev Gastroenterol Hepatol. 2019 г.; 16 : 7-18
-
Секреторният IgA медиира ретротрансцитозата на непокътнати глиадинови пептиди чрез трансфериновия рецептор при целиакия.
J Exp. Med. 2008 г.; 205 : 143-154
-
Тъканната трансглутаминаза селективно модифицира глиадиновите пептиди, които се разпознават от произхождащите от червата Т клетки при цьолиакия.
Nat Med. 1998 г.; 4 : 713-717
-
Уникална подгрупа дендритни клетки се натрупва в лезията на целиакия и ефективно активира глутен-реактивните Т клетки.
Гастроентерология. 2006 г.; 131 : 428-438
-
Бързо натрупване на CD14 + CD11c + дендритни клетки в чревната лигавица на цьолиакия след in vivo предизвикване с глутен.
PLoS One. 2012 г.; 7 : 1-10
-
Пряка роля за взаимодействието NKG2D/MICA при атрофия на вилози по време на целиакия.
Имунитет. 2004 г.; 21 : 367-377
-
Широка експресия на MICA/B в лигавицата на тънките черва: връзка между клетъчния стрес и целиакията.
PLoS One. 2013 г.; 8 e73658
-
IL-15 функционира като сигнал за опасност за регулиране на Т клетките, живеещи в тъканите, и разрушаването на тъканите.
Nat Rev Immunol. 2015 г.; 15 : 771-783
-
Доказателство, че патогенната трансглутаминаза 2 при целиакия произлиза от ентероцити.
Гастроентерология. 2020 г.; 159 : 788-790
-
Плазмените клетки са най-разпространените клетки, експресиращи глутенов пептид MHC във възпалени чревни тъкани от пациенти с целиакия.
Гастроентерология. 2019 г.; 156 : 1428-1439
-
HLA-DR, DP и DQ експресия в тънките черва на пациенти с целиакия.
Clin Exp Immunol. 1987 г.; 70 : 386-393
-
Човешки чревни ентероиди моделират MHC-II в чревния епител.
Преден имунол. 2019 г.; 10 : 1-8
-
HLA-DQ определя реакцията към екзогенни пшенични протеини: модел на чувствителност към глутен при трансгенни нокаут мишки.
J Immunol. 2002 г.; 169 : 5595-5600
-
Резистентност към целиакия при хуманизирани HLA-DR3-DQ2-трансгенни мишки, експресиращи специфични анти-глиадин CD4 + Т клетки.
J Immunol. 2009 г.; 182 : 7440-7450
-
Сенсибилизацията към глиадин индуцира умерена ентеропатия и инсулит при диабетични DQ8 мишки без затлъстяване.
J Immunol. 2011 г.; 187 : 4338-4346
-
Интраепителни лимфоцити във върха на вилата: показват ли потенциална цьолиакия?.
J Clin Pathol. 2004 г.; 57 : 835-839
-
Разработване на първична монослойна културална система от чревни епителни клетки на мишка за оценка на факторите, които модулират IgA трансцитозата.
Мукозен имунол. 2014 г.; 7 : 818-828
-
Дългосрочно разширяване на епителни органоиди от човешко дебело черво, аденом, аденокарцином и епител на Барет.
Гастроентерология. 2011 г.; 141 : 1762-1772
-
Към системно разбиране на MHC клас I и MHC клас II антигенно представяне.
Nat Rev Immunol. 2011 г.; 11 : 823-836
-
Селективно разширяване на интраепителни лимфоцити, експресиращи HLA-E-специфичния естествен убиец рецептор CD94 при целиакия.
Гастроентерология. 2000 г.; 118 : 867-879
-
Освобождаване на цитокини и стомашно-чревни симптоми след предизвикване на глутен при целиакия.
Sci Adv. 2019 г.; 5 eaaw7756
-
Ролята на хемокините в набирането на лимфоцити в черния дроб.
Dig Dis. 2010 г.; 28 : 31-44
-
Серумните цитокини са повишени по време на медиирано от глутен освобождаване на цитокини при целиакия.
Clin Exp Immunol. 2019 г.; 199 : 68-78
-
Цьолиакия: трябва ли да ни е грижа за микробите?.
Am J Physiol Gastrointest Liver Physiol. 2019 г.; 317 : G161-G170
-
Дуоденалните бактерии от пациенти с цьолиакия и здрави индивиди ясно влияят върху разграждането на глутена и имуногенността.
Гастроентерология. 2016 г.; 151 : 670-783
-
Експресия на епителен MHC клас II и нейната роля в представянето на антиген в стомашно-чревния и респираторния тракт.
Преден имунол. 2018 г.; 9 : 1-14
-
Защо чревните епителни клетки експресират MHC клас II?.
Имунология. 2021 г.; 162 : 357-367
-
Повишена експресия на HLA-DR от ентероцити при деца с целиакия.
Гастроентерология. 1986 г.; 91 : 1206-1212
-
Цитокините на Т хелперните клетки модулират обновяването и диференциацията на чревните стволови клетки.
клетка. 2018 г.; 175 : 1307-1320.e22
-
Чревната епителна експресия на MHCII определя тежестта на химичния, Т-клетъчно индуциран и инфекциозен колит при мишки.
Гастроентерология. 2020 г.; 159 : 1342-1356.e6
-
Интерферон-γ индуцира експресия на МНС клас II върху чревни епителни клетки и предпазва мишките от колит.
PLoS One. 2014 г.; 9 e86844
-
Представянето на MHC клас II антиген от чревния епител инициира болестта присадка срещу гостоприемник и се влияе от микробиотата.
Имунитет. 2019 г.; 51 : 885-898.e7
-
Цьолиакия.
Ланцет. 2003 г.; 362 : 383-391
-
Глиадин-специфични, HLA-DQ(α1∗0501, β1∗0201) ограничени Т клетки, изолирани от лигавицата на тънките черва на пациенти с целиакия.
J Exp Med. 1993 г.; 178 : 187-196
-
Т-клетъчният отговор към глутен при пациенти с HLA-DQ2.2 разкрива изискване за стабилност на пептид-МНС при целиакия.
Гастроентерология. 2012 г.; 142 : 552-561
-
Структурна основа за HLA-DQ2-медиирано представяне на глутенови епитопи при целиакия.
Proc Natl Acad Sci US A. 2004; 101 : 4175-4179
-
IL-15, глутен и HLA-DQ8 стимулират разрушаването на тъканите при целиакия.
Природата. 2020 г.; 578 : 600-608
-
MHC клас II антигенно представяне от чревни епителни клетки фино настройва бактериално-реактивните CD4 Т клетъчни отговори.
Мукозен имунол. 2024 г.; 17 : 416-430
-
Епителната IFNγ сигнализация и компартментализираното представяне на антиген организират чревния имунитет.
Природата. 2023 г.; 623 : 1044-1052
-
Биологията на интерлевкин-2.
Annu Rev Immunol. 2008 г.; 26 : 453-479
-
Глутенът индуцира чревен цитокинов отговор, силно доминиран от интерферон гама при пациенти с целиакия.
Гастроентерология. 1998 г.; 115 : 551-563
-
Освобождаването на цитокини след поглъщане на глутен разграничава цьолиакията от самооценената чувствителност към глутен.
United European Gastroenterol J. 2020; 8 : 108-118
-
Повишаване на серумните цитокини при целиакия: връзка с представянето на заболяването.
Hum Immunol. 2010 г.; 71 : 50-57
-
Интерлевкин 15, получен от епител, регулира производството на Th1 цитокини в интраепителните лимфоцити, цитотоксичността и преживяемостта при целиакия.
червата. 2006 г.; 55 : 469-477
-
Хемокиновата система във вродения имунитет.
Cold Spring Harb Perspect Biol. 2015 г.; 7 a106303
-
Роля на оста CXCR3/CXCL10 в набирането на имунни клетки в тънките черва при целиакия.
PLoS One. 2014 г.; 9 : 1-12
-
Биогеографски вариации и функционални пътища на чревната микробиота при целиакия.
Гастроентерология. 2022 г.; 163 : 1351-1363.e15
-
Чревна ex vivo органоидна култура разкрива променени програмирани стволови клетки на криптите при пациенти с целиакия.
Sci Rep. 2020; 10 : 1-10
-
Органоидите, получени от човешки черва, осигуряват модел за изследване на реакцията на глутен и ефектите на молекули, получени от микробиота, при целиакия.
Sci Rep. 2019; 9 : 7029
-
Чревният епител модулира реакцията на макрофагите към глиадин при целиакия.
Преден Nutr. 2019 г.; 6 : 167
-
Чревните епителни екзозоми носят МНС клас II/пептиди, способни да информират имунната система при мишки.
червата. 2003 г.; 52 : 1690-1697













